Купирование болевого синдрома — есть ли альтернатива НПВС?
Рубрика:
Болевой синдром
Цель исследования: разработать схему консервативной терапии при обострении остеоартроза для минимизации нежелательных эффектов от приема нестероидных противовоспалительных средств (НПВС).
Материал и методы: в исследование включены 358 пациентов (возраст — 31–82 года), страдающих остеоартрозом коленного сустава I–III степени в стадии обострения с болевым синдромом 48–83 балла по визуальной аналоговой шкале (ВАШ). Пациенты были разделены на 3 группы: 1-я группа (n=96) принимала диклофенак 150 мг/сут; 2-я группа (n=52) — Траумель® С по 1 таблетке 3 р./сут; 3-я группа (n=209) получала комплексную терапию: диклофенак
100 мг/сут + Траумель® С (по 1 таблетке 3 р./сут). Длительность наблюдения — 1 мес. При снижении боли по шкале ВАШ до 15 баллов НПВС отменялись.
Результаты и обсуждение: в 1-й группе в 1-й день среднее значение болевого синдрома снизилось на 16,2 балла по ВАШ, к 3 сут — достигло 24,5 балла. НПВС отменены к 3 сут у 23 пациентов, к 4 сут — еще у 22, к 7 сут — у всех пациентов. Во 2-й группе снижение болевого синдрома происходило медленнее (в первые 3 сут — на 9,9 балла), к 4 и 5 сут — на 22 и 30,2 балла соответственно. К концу наблюдения средний показатель составил 8,6 балла. В 3-й группе в 1 сут отмечалось снижение боли на 17,3 балла. К 3 сут показатель был сопоставим с эффектом в 1-й группе, у 20 человек отменены НПВС. К 4 и 5 сут средние показатели боли в 3-й группе были меньше, чем в 1-й. К 6 сут НПВС отменены всем пациентам. Средняя суммарная доза НПВС составила в 1-й группе 492 мг, а в 3-й группе — 307 мг.
Выводы: совместный прием НПВС и препарата Траумель® С позволяет добиться быстрого и устойчивого терапевтического эффекта на фоне снижения суммарной дозы НПВС по сравнению с монотерапией в 1,6 раза.
Ключевые слова: остеоартроз, болевой синдром, визуальная аналоговая шкала (ВАШ), нестероидные противовоспалительные средства (НПВС), Траумель® С.
Материал и методы: в исследование включены 358 пациентов (возраст — 31–82 года), страдающих остеоартрозом коленного сустава I–III степени в стадии обострения с болевым синдромом 48–83 балла по визуальной аналоговой шкале (ВАШ). Пациенты были разделены на 3 группы: 1-я группа (n=96) принимала диклофенак 150 мг/сут; 2-я группа (n=52) — Траумель® С по 1 таблетке 3 р./сут; 3-я группа (n=209) получала комплексную терапию: диклофенак
100 мг/сут + Траумель® С (по 1 таблетке 3 р./сут). Длительность наблюдения — 1 мес. При снижении боли по шкале ВАШ до 15 баллов НПВС отменялись.
Результаты и обсуждение: в 1-й группе в 1-й день среднее значение болевого синдрома снизилось на 16,2 балла по ВАШ, к 3 сут — достигло 24,5 балла. НПВС отменены к 3 сут у 23 пациентов, к 4 сут — еще у 22, к 7 сут — у всех пациентов. Во 2-й группе снижение болевого синдрома происходило медленнее (в первые 3 сут — на 9,9 балла), к 4 и 5 сут — на 22 и 30,2 балла соответственно. К концу наблюдения средний показатель составил 8,6 балла. В 3-й группе в 1 сут отмечалось снижение боли на 17,3 балла. К 3 сут показатель был сопоставим с эффектом в 1-й группе, у 20 человек отменены НПВС. К 4 и 5 сут средние показатели боли в 3-й группе были меньше, чем в 1-й. К 6 сут НПВС отменены всем пациентам. Средняя суммарная доза НПВС составила в 1-й группе 492 мг, а в 3-й группе — 307 мг.
Выводы: совместный прием НПВС и препарата Траумель® С позволяет добиться быстрого и устойчивого терапевтического эффекта на фоне снижения суммарной дозы НПВС по сравнению с монотерапией в 1,6 раза.
Ключевые слова: остеоартроз, болевой синдром, визуальная аналоговая шкала (ВАШ), нестероидные противовоспалительные средства (НПВС), Траумель® С.
A.V. Garkavi1, G.M. Kavalerskiy1, S.V.Terekhin1, V.A. Meshcheryakov2
1 Sechenov University, Moscow
2 Ruza District Hospital
Aim: to develop a scheme of conservative therapy of exacerbation of osteoarthrosis to minimize the NSAIDs side effects.
Patients and Methods: 358 patients (age 31–82) with osteoarthrosis of the knee joint of I–III degree in the acute stage with
a pain syndrome of 48–83 points on a visual analogue scale (VAS) were included in the study. Patients were divided into
3 groups: group 1 (n = 96) received diclofenac 150 mg / day; group 2 (n = 52) received Traumeel S for 1 tablet 3 times
a day; group 3 (n = 209) received a complex therapy: diclofenac 100 mg / day + Traumeel S (1 t х 3 times a day). The duration
of observation was 1 month. With a decrease in pain up to 15 points on the VAS scale NSAIDs were cancelled.
Results and Discussion: in group 1 on the 1st day the average value of the pain syndrome decreased by 16.2 points by VAS, on the 3d day it reached 24.5 points. By the 3d day NSAIDs were canceled for 23 patients, by the 4th day — for 22 patients more, by the 7th day — for all the patients. In group 2, the pain syndrome decreased more slowly (by 9.9 points during the first
3 days), by the 4th and 5th days it decreased by 22 and 30.2 points, respectively. By the end of the observation, the average score was 8.6 points. In the third group: for the 1st day the pain decreased by 17.3 points. By the 3d day the value was comparable to the effect in group 1, NSAIDs were cancelled for 20 patients. By the 4th and 5th days the average pain value in group 3 was lower than in group 1. By the 6th day NSAIDs were cancelled for all the patients. The average total dose of NSAIDs was 492 mg in group 1, and 307 mg in group 3.
Conclusions: a combined treatment with NSAIDs and Traumeel S allows to achieve a rapid and stable therapeutic effect with reduction of the total dose of NSAIDs by a factor of 1.6 in comparison with monotherapy.
Key words: osteoarthrosis, pain syndrome, visual analogue scale (VAS), non-steroidal anti-inflammatory drugs (NSAIDs), Traumeel S.
For citation: Garkavi A.V., Kavalerskiy G.M., Terekhin S.V., Meshcheryakov V.A. The informative value of diagnostic tests
in urogenital tuberculosis screening // RMJ. Medical Review. 2018. № 1(I). P. 50–53.
Статья посвящена возможностям купирования болевого синдрома и поиску альтернативы НПВС. Показано, что совместный прием НПВС и препарата Траумель С позволяет добиться быстрого и устойчивого терапевтического эффекта на фоне снижения суммарной дозы НПВС.
 Боль и воспаление — постоянные и неотъемлемые проявления подавляющего большинства патологических состояний человеческого организма. При поражениях опорно-двигательной системы они обязательно имеют место как при острой травме, так и при хронических заболеваниях. Одно из самых распространенных в мире заболеваний опорно-двигательной системы — остеоартроз постоянно остается в центре внимания как ученых, так и практических врачей [1, 2]. Контингент пациентов, обращающихся за медицинской помощью по этому поводу, на рубеже ХХ и XXI вв. несколько изменился. Если раньше преобладание пациентов пожилого и старческого возраста было подавляющим (по некоторым оценкам, до 80% и более), то сегодня остеоартроз заметно «помолодел». Все чаще патологию суставов выявляют у лиц трудоспособного возраста, порой у совсем молодых [1, 3, 4]. Связано это, по-видимому, как с ростом физических (прежде всего спортивных) нагрузок, так и с существенно возросшими диагностическими возможностями современной медицины, когда диагноз остеоартроза удается верифицировать на самых ранних стадиях.
Боль и воспаление — постоянные и неотъемлемые проявления подавляющего большинства патологических состояний человеческого организма. При поражениях опорно-двигательной системы они обязательно имеют место как при острой травме, так и при хронических заболеваниях. Одно из самых распространенных в мире заболеваний опорно-двигательной системы — остеоартроз постоянно остается в центре внимания как ученых, так и практических врачей [1, 2]. Контингент пациентов, обращающихся за медицинской помощью по этому поводу, на рубеже ХХ и XXI вв. несколько изменился. Если раньше преобладание пациентов пожилого и старческого возраста было подавляющим (по некоторым оценкам, до 80% и более), то сегодня остеоартроз заметно «помолодел». Все чаще патологию суставов выявляют у лиц трудоспособного возраста, порой у совсем молодых [1, 3, 4]. Связано это, по-видимому, как с ростом физических (прежде всего спортивных) нагрузок, так и с существенно возросшими диагностическими возможностями современной медицины, когда диагноз остеоартроза удается верифицировать на самых ранних стадиях.Так или иначе, проблема лечения остеоартроза в значительной степени приобретает сегодня не только медицинское, но и социально-экономическое значение ввиду того, что заболевание поражает существенную часть трудоспособного населения [5].
Авторы многочисленных публикаций, посвященных диагностике и лечению остеоартроза, в большинстве своем сходятся во мнении, что необходим комплексный подход, гармонично сочетающий несколько известных методов — как консервативных, так и оперативных. Однако при любой выбранной лечебной стратегии, вплоть до эндопротезирования, практически все пациенты принимают медикаменты, имеющие противовоспалительное и противоболевое действие [5–7].
В этом кроется большая опасность. Болевой синдром — обязательное проявление остеоартроза. В ряде случаев, особенно на сравнительно ранних стадиях развития патологического процесса, пациенты вообще не предъявляют никаких жалоб — только на боль. И именно болевые ощущения заставляют их начать лечение. Однако, к сожалению, медикаментозную терапию они часто назначают себе сами, черпая сведения из рекламных объявлений или получая советы знакомых. Самыми известными, распространенными и эффективными препаратами соответствующего действия являются нестероидные противовоспалительные средства (НПВС). Причем для пациентов при выборе лекарства его эффективность является абсолютно определяющим, а порой и единственным фактором. Задуматься о безопасности такого бесконтрольного лечения заставляют только признаки начавшихся осложнений. Для НПВС наиболее характерны осложнения со стороны желудочно-кишечного тракта (вплоть до язвенного кровотечения), однако описано их негативное воздействие и на другие органы и системы [8, 9].
По характеру своего действия НПВС отличаются своим влиянием (ингибицией) на циклооксигеназы. Самые быстродействующие и эффективные препараты (неселективные ингибиторы ЦОГ-1 и ЦОГ-2) имеют и наибольшую опасность побочных эффектов, поэтому рекомендованная продолжительность курса лечения обычно не превышает 7–10 дней. У селективных ингибиторов ЦОГ-2 доступен более продолжительный курс (до 3 нед. и более), однако их эффективность (и прежде всего — быстродействие) несколько ниже. Большинство пациентов этого не знают, что приводит к употреблению НПВС бесконтрольно и в течение длительного времени [8–11].
Можно сказать, что самолечение опасно всегда, и это правда. Однако даже врач, зная о возможных нежелательных эффектах приема НПВС, в большинстве случаев все-таки вынужден их назначать. К сожалению, НПВС до сих пор наиболее эффективны при обострении остеоартроза. Конечно, врач старается минимизировать побочные эффекты, выбирая селективные ингибиторы ЦОГ-2, назначая гастропротективные препараты для защиты слизистой желудочно-кишечного тракта от повреждения (ингибиторы протонной помпы) или пытаясь найти замену НПВС. Однако «защитники» все же не обеспечивают 100% защиты, а прочие препараты противовоспалительного и анальгетического действия (биологически активные добавки, хондропротекторы) не столь эффективны, особенно на фоне острого воспаления [2, 5, 8, 11].
В результате мы часто сталкиваемся, особенно у пожилых пациентов, имеющих многолетний анамнез, не с потенциальной опасностью осложнений, а с прямыми противопоказаниями к приему НПВС на фоне уже развившихся вследствие такого приема соматических заболеваний.
Положение становится безвыходным. Даже если определяют показания к оперативному лечению (артроскопия, хондропластика, остеотомия, эндопротезирование), пациент стремится в ожидании операции все же избавиться от постоянной боли или хотя бы снизить ее интенсивность. И в качестве альтернативы прибегают к внутрисуставному введению кортикостероидов. Это дает временное улучшение, но вместе с тем ведет к быстрому нарастанию деструктивных процессов в суставе [2, 5, 10].
Таким образом, вопрос о том, есть ли приемлемая альтернатива приему НПВС при острой воспалительной реакции на фоне остеоартроза, представляет несомненный практический интерес.
Целью нашей работы было разработать схему консервативной терапии острой болевой и воспалительной реакции при остеоартрозе, позволяющую минимизировать нежелательные эффекты от приема НПВС.
Материал и методы
Под наблюдением находились 358 пациентов в возрасте от 31 до 82 лет (средний возраст — 56,8 года), страдающих остеоартрозом коленного сустава I–III степени тяжести по рентгенологической классификации Kellgren — Lawrence. Давность анамнеза составила от 2,5 до 18 лет. Для верификации диагноза всем были выполнены рентгенограммы в стандартных проекциях. Кроме рентгенограмм 196 пациентам (54,7%) выполнено МРТ-исследование, 98 (27,4%) — УЗИ, 35 (9,8%) — КТ. У всех патологический процесс был к началу лечения в стадии обострения, что сопровождалось болевым синдромом от 48 до 83 баллов по 100-балльной визуальной аналоговой шкале (ВАШ) и выраженной дисфункцией.Пациенты с IV степенью тяжести не вошли в наше исследование, т. к. у них остеоартроз сопровождался выраженными анатомическими деформациями костных структур, значительными нарушениями биомеханики ходьбы, что не позволяло объективно оценить эффект медикаментозной терапии. Им были определены показания к эндопротезированию.
Пациенты были разделены на 3 группы. В каждой группе с первого дня начинали проводить противовоспалительную терапию. Показанием для прекращения приема НПВС считали снижение болевого синдрома до 15 баллов по ВАШ, что соответствовало оценке «незначительная боль».
Помимо НПВС мы применяли препарат Траумель® С, противовоспалительное действие которого достаточно давно известно и описано в ряде публикаций, в т. ч. в материалах EULAR [12, 13]. Никакой другой терапии в этот период не проводили.
Пациентам 1-й группы (n=96) с первого дня назначали диклофенак (150 мг/сут) в капсулах с параллельным приемом препарата омепразол 40 мг/сут в качестве протектора.
Пациентам 2-й группы (n=52) с первого дня назначали Траумель® С по 1 таблетке 3 р./сут. С учетом его заведомо менее быстрого действия монотерапию с применением Траумеля С проводили пациентам с болевым синдромом, не превышающим 55 баллов по ВАШ.
В 3-й группе (n=209) применяли комплексную терапию, сочетая диклофенак и Траумель® С. С первого дня назначали параллельно диклофенак (100 мг/сут) + омепразол (40 мг/сут) + Траумель® С (1 таблетка 3 р./сут). После снижения интенсивности болевого синдрома до 15 баллов по ВАШ оставляли только Траумель® С в дозировке 1 таблетка 2 р./сут, продолжая этот курс до 1 мес.
Наблюдение проводили в течение 1 мес., фиксируя уровень болевого синдрома по ВАШ: в первую неделю — ежедневно, далее — 1 раз в 5 дней. Фиксировали боль в различных ситуациях: после длительной неподвижности или сна («стартовая»), при нагрузке (ходьбе), в покое, а также ночные боли. В качестве контрольного показателя выбирали боль наибольшей интенсивности.
Результаты и обсуждение
Во всех группах получена отчетливая положительная динамика, однако каждая группа имела свои особенности (рис. 1).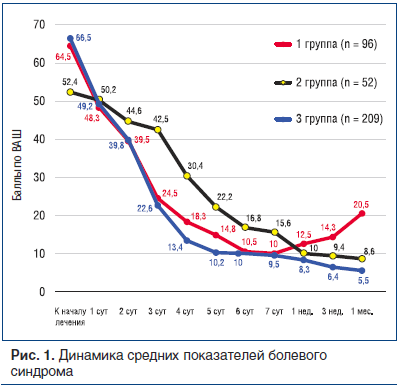
В 1-й группе в первый же день достигнуто существенное снижение среднего значения болевого синдрома (на 16,2 балла по ВАШ). Далее это снижение продолжилось такими же темпами. К 3 сут средний показатель составил 24,5 балла по ВАШ, причем 23 человека (24,0%) оценили боль ниже 15 баллов, в связи с чем прием НПВС был прекращен, однако наблюдение продолжено. К 4 сут боль ниже 15 баллов отмечена еще у 22 человек (всего 45 случаев, или 46,9%), и к 7 сут прием НПВС был отменен у всех пациентов (рис. 2).
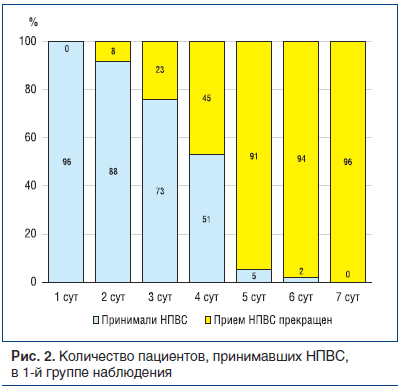
В то же время после отмены НПВС боль у некоторых пациентов несколько возросла, что к концу 1 мес. наблюдения дало рост среднего показателя на 10,5 балла по сравнению с минимальным значением, зафиксированным на момент отмены препарата.
Во 2-й группе вначале снижение интенсивности болевого синдрома происходило значительно медленнее (в первые 3 сут — всего на 9,9 балла), однако с учетом того, что прием препарата Траумель® С продолжался в течение всего месяца наблюдения, боль все время продолжала уменьшаться. Значительное снижение интенсивности боли относительно начального уровня достигнуто только к 4 сут (на 22 балла) и 5 сут (на 30,2 балла). К концу наблюдения 35 пациентов (67,3%) вообще не ощущали боли, а средний показатель составил 8,6 балла (незначительная боль).
В 3-й группе при одновременном приеме препаратов проявился эффект каждого из них. Уже через сутки отмечено существенное снижение среднего показателя боли (на 17,3 балла). К 3 сут средний показатель был практически таким же, как в 1-й группе, а у 20 человек (9,6%) снижение интенсивности боли до отметки менее 15 баллов позволило прекратить прием НПВС. К 4 и 5 сут средние показатели боли в 3-й группе были меньше, чем в 1-й группе, соответственно на 4,9 и 4,6 балла, а количество пациентов, прекративших прием НПВС, составило соответственно
125 (59,8%) и 206 (98,6%). К 6 сут прием НПВС отменен у всех пациентов (рис. 3).
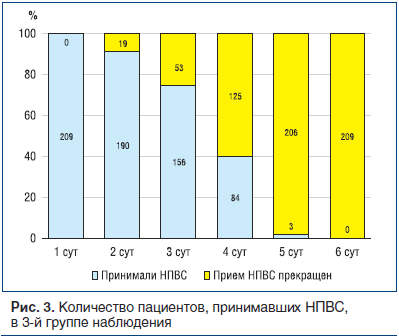
Оценивая достигнутый обезболивающий эффект в группах наблюдения, следует учесть, что изначально интенсивность боли во 2-й группе была существенно ниже, чем в 1-й и 3-й группах, т. к. при определении групп мы принимали во внимание более медленное действие препарата Траумель® С. В связи с этим 2-я группа была сформирована из пациентов, имевших среднее значение болевого синдрома 52,4, тогда как в других группах оно составило 64,5 (1-я группа) и 66,5 (3-я группа).
Поэтому для того, чтобы получить более полное представление о сравнительной эффективности препаратов, мы в каждой группе проанализировали снижение интенсивности боли в процентном отношении к начальному уровню (рис. 4).
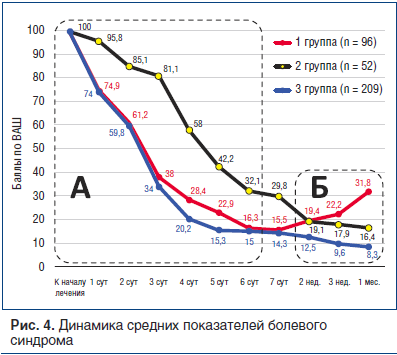
Сравнение показало, что монотерапия препаратом Траумель® С (2-я группа) в первые 3 сут имеет достаточно низкую эффективность, затем темп снижения боли увеличивается, но все равно существенно уступает аналогичным показателям в 1-й и 3-й группах, в которых пациенты получали НПВС (область А на рис. 4). В то же время в 1-й группе, где проводилась монотерапия с применением НПВС, после отмены препарата отмечен существенный рост среднего показателя боли, тогда как во 2-й и 3-й группах, где пациенты продолжали получать Траумель® С, боль продолжала уменьшаться (область Б на рис. 4).
При сравнении результатов лечения в 1-й и 3-й группах следует обратить внимание на суммарную дозу НПВС, которую получили пациенты. В 1-й группе суточная доза составила 150 мг, а в 3-й группе — 100 мг. Кроме того, в 1-й группе средняя продолжительность курса приема НПВС составила 3,3 дня, а в 3-й группе — 3,1 дня. Таким образом, средняя суммарная доза НПВС составила в 1-й группе 492 мг, а в 3-й группе — 307 мг, что в 1,6 раза меньше (р<0,001).
Выводы:
Выраженный болевой синдром у пациентов с обострением гонартроза можно существенно снизить с помощью медикаментозной противовоспалительной терапии.Пероральный прием НПВС — неселективных ингибиторов ЦОГ позволяет добиться выраженного положительного эффекта уже в первые сутки, однако длительный курс чреват развитием нежелательных побочных эффектов, а после отмены препарата отмечается некоторый регресс.
Пероральный прием препарата Траумель® С в первые 3 сут обладает меньшей эффективностью, однако в дальнейшем темп снижения интенсивности боли возрастает, она продолжает уменьшаться на протяжении всего времени приема препарата.
Одновременный прием НПВС и Траумеля С позволяет сочетать вышеописанные эффекты и добиться лучших результатов, чем при монотерапии, снизив при этом дозу НПВС в 1,6 раза (р<0,001).
Литература
1. Миронов С. П., Омельяненко Н. П., Орлецкий А. К. и др. Остеоартроз: современное состояние проблемы (аналитический обзор) // Вестник травматологии и ортопедии им. Н. Н. Приорова. 2001. № 2. С. 96–99 [Mironov S.P., Omel’janenko N.P., Orleckij A. K. i dr. Osteoartroz: sovremennoe sostojanie problemy (analiticheskij obzor) // Vestnik travmatologii i ortopedii im. N. N. Priorova. 2001. № 2. С. 96–99 (in Russian)].
2. Пихлак А. Э., Гаркави А. В., Логачев В. А., Терешенков В. П. Остеоартроз: клиника, диагностика, лечение. Учебное пособие для врачей. М.: ИД «Медпрактика-М», 2013. 144 с. [Pikhlak A.E., Garkavi A. V., Logachev V. A., Tereshenkov V. P. Osteoartroz: klinika, diagnostika, lecheniye. Uchebnoye posobiye dlya vrachey. M.: ID «Medpraktika-M», 2013. 144 s. (in Russian)].
3. Harrysson O. L., Robertsson O., Nayfeh F. Higher cumulative revision rate of knee arthroplasties in younger patients with osteoarthritis // Clin.Orthop. 2008. Vol. 421. P. 162–168.
4. National Joint Registry (United Kingdom) — 8th Annual report. 2011. 70 p.
5. Алексеева Л. И., Зайцева Е. М. Клинические подходы к лечению остеоартроза // Русский медицинский журнал. 2006. Т. 14. № 6 (258). С. 450–453 [Alekseeva L.I., Zajceva E. M. Klinicheskie podhody k lecheniju osteoartroza // Russkij medicinskij zhurnal. 2006. T. 14. № 6 (258). S. 450–453 (in Russian)].
6. Багирова Г. Г., Майко О. Ю. Остеоартроз: эпидемиология, клиника, диагностика, лечение. М.: Арнебия, 2005. 224 с. [Bagirova G.G., Majko O. Ju. Osteoartroz: jepidemiologija, klinika, diagnostika, lechenie. M.: Arnebija, 2005. 224 s. (in Russian)].
7. Носков С. М. Консервативное лечение остеоартроза. М.: ГЭОТАР-Медиа, 2012. 208 с. [Noskov S. M. Konservativnoe lechenie osteoartroza. М.: GJeOTAR-Media, 2012. 208 s. (in Russian)].
8. Каратеев А. Е. Гастродуоденальная безопасность селективных ингибиторов циклооксигеназы-2: проверка практикой // Терапевтический архив. 2005. № 5. С. 69–72 [Karateev A. E. Gastroduodenal’naja bezopasnost’ selektivnyh ingibitorov ciklooksigenazy-2: proverka praktikoj // Terapevticheskij arhiv. 2005. № 5. S. 69–72 (in Russian)].
9. Коршунов Н. И., Ершова О. Б. Современные подходы к фармакотерапии остеоартроза // Consilium medicum. 2006. № 2. С. 34–38 [Korshunov N.I., Ershova O. B. Sovremennye podhody k farmakoterapii osteoartroza // Consilium medicum. 2006. № 2. S. 34–38 (in Russian)].
10. Лила А. М. Современная фармакотерапия остеоартроза // Terra medica. 2005. № 1 (37). C. 3–9 [Lila A. M. Sovremennaja farmakoterapija osteoartroza // Terra medica. 2005. № 1 (37). S. 3–9 (in Russian)].
11. Ding C. Do NSAID affect the progression of osteoarthritis? // Inflammation. 2002. Vol. 26 (3). P. 139–142.
12. Lozada C., del Rio E., Reitberg D.P. et al. Risk benefit of co-administered Traumeel® (Tr14) and Zeel® (Ze14) intra-articular (IA) injections in patients with moderate-to-severe pain associated with OA of the knee (OAK) (THU0441) //Ann. Rheum. Dis. 2015. Vol. 74. Suppl. 2. P. 4268.
13. St. Laurent III G., Seilheimer B., Tackett M. et al. Deep sequencing transcriptome analysis of the effect of Traumeel versus diclofenac therapeutic action in wound healing // Ann Rheum Dis. 2017. Vol. 76. Suppl. 2. P. 202.
2. Пихлак А. Э., Гаркави А. В., Логачев В. А., Терешенков В. П. Остеоартроз: клиника, диагностика, лечение. Учебное пособие для врачей. М.: ИД «Медпрактика-М», 2013. 144 с. [Pikhlak A.E., Garkavi A. V., Logachev V. A., Tereshenkov V. P. Osteoartroz: klinika, diagnostika, lecheniye. Uchebnoye posobiye dlya vrachey. M.: ID «Medpraktika-M», 2013. 144 s. (in Russian)].
3. Harrysson O. L., Robertsson O., Nayfeh F. Higher cumulative revision rate of knee arthroplasties in younger patients with osteoarthritis // Clin.Orthop. 2008. Vol. 421. P. 162–168.
4. National Joint Registry (United Kingdom) — 8th Annual report. 2011. 70 p.
5. Алексеева Л. И., Зайцева Е. М. Клинические подходы к лечению остеоартроза // Русский медицинский журнал. 2006. Т. 14. № 6 (258). С. 450–453 [Alekseeva L.I., Zajceva E. M. Klinicheskie podhody k lecheniju osteoartroza // Russkij medicinskij zhurnal. 2006. T. 14. № 6 (258). S. 450–453 (in Russian)].
6. Багирова Г. Г., Майко О. Ю. Остеоартроз: эпидемиология, клиника, диагностика, лечение. М.: Арнебия, 2005. 224 с. [Bagirova G.G., Majko O. Ju. Osteoartroz: jepidemiologija, klinika, diagnostika, lechenie. M.: Arnebija, 2005. 224 s. (in Russian)].
7. Носков С. М. Консервативное лечение остеоартроза. М.: ГЭОТАР-Медиа, 2012. 208 с. [Noskov S. M. Konservativnoe lechenie osteoartroza. М.: GJeOTAR-Media, 2012. 208 s. (in Russian)].
8. Каратеев А. Е. Гастродуоденальная безопасность селективных ингибиторов циклооксигеназы-2: проверка практикой // Терапевтический архив. 2005. № 5. С. 69–72 [Karateev A. E. Gastroduodenal’naja bezopasnost’ selektivnyh ingibitorov ciklooksigenazy-2: proverka praktikoj // Terapevticheskij arhiv. 2005. № 5. S. 69–72 (in Russian)].
9. Коршунов Н. И., Ершова О. Б. Современные подходы к фармакотерапии остеоартроза // Consilium medicum. 2006. № 2. С. 34–38 [Korshunov N.I., Ershova O. B. Sovremennye podhody k farmakoterapii osteoartroza // Consilium medicum. 2006. № 2. S. 34–38 (in Russian)].
10. Лила А. М. Современная фармакотерапия остеоартроза // Terra medica. 2005. № 1 (37). C. 3–9 [Lila A. M. Sovremennaja farmakoterapija osteoartroza // Terra medica. 2005. № 1 (37). S. 3–9 (in Russian)].
11. Ding C. Do NSAID affect the progression of osteoarthritis? // Inflammation. 2002. Vol. 26 (3). P. 139–142.
12. Lozada C., del Rio E., Reitberg D.P. et al. Risk benefit of co-administered Traumeel® (Tr14) and Zeel® (Ze14) intra-articular (IA) injections in patients with moderate-to-severe pain associated with OA of the knee (OAK) (THU0441) //Ann. Rheum. Dis. 2015. Vol. 74. Suppl. 2. P. 4268.
13. St. Laurent III G., Seilheimer B., Tackett M. et al. Deep sequencing transcriptome analysis of the effect of Traumeel versus diclofenac therapeutic action in wound healing // Ann Rheum Dis. 2017. Vol. 76. Suppl. 2. P. 202.

Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Предыдущая статья
Следующая статья
